1、RT-PCR检测
实验原理
带荧光标记的寡核苷酸探针分子小,偏振光弱。当探针与 DNA 上的特异片段结合后分子量增大,偏振光增强。在 PCR 扩增时,随着引物介导的新链形成,探针从模板上解离下来,重新成为游离状态,偏振光又减弱。
在每一个 PCR 循环退火阶段,探针又可与 DNA 链重新配对,偏振光增强。在此阶段检测偏振光的增值,可对其进行定量检测。而当所扩增的核酸序列中不含与探针相配对的特定 DNA 片段时,荧光探针无法与核酸序列配对,其荧光偏振值很弱。故可检测扩增核苷酸序列中是否含有目的 DNA 片段。
我司提供
组织细胞miRNA/lncRNA/circRNA RT-qPCR实验,外泌体miRNA RT-qPCR实验,CHIP-qPCR实验,RIP-qPCR实验,MeRIP-qPCR实验。
2、WB检测
蛋白质印迹法(免疫印迹试验)即Western blot,是将电泳分离后的细胞或组织总蛋白质从凝胶转移到固相支持物NC膜或PVDF膜上,然后用特异性抗体检测某特定抗原的一种蛋白质检测技术,现已广泛应用于基因在蛋白水平的表达研究。
通过抗原抗体反应对目标蛋白的表达进行半定量检测,还用于蛋白-蛋白、蛋白-DNA的相互作用的后续分析。
实验原理:
Western blot(WB)是将蛋白样本通过聚丙烯酰胺电泳按分子量大小分离,再转移到杂交膜(blot)上,然后通过一抗/二抗复合物对靶蛋白进行特异性检测的方法。其基本原理是通过特异性抗体对凝胶电泳处理过的细胞或生物组织样品进行着色。
通过分析着色的位置和着色深度获得特定蛋白质在所分析的细胞或组织中表达情况的信息。
实验流程:
WB一般步骤:蛋白质抽提,蛋白质定量,变性聚丙烯酰胺不连续凝胶电泳(SDS-PAGE),蛋白质转移,Western blot膜的封闭和抗体孵育,Western blot结果检测,Western blot数据分析。
基安生物可提供:
组织细胞样本WB实验,外泌体样本WB实验,RNA PULL DOWN WB实验。
WB结果展示图:
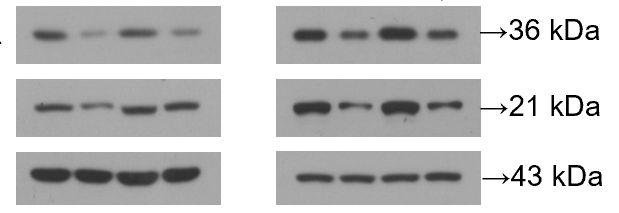
3、细胞增殖
细胞增殖—一个基础而关键的细胞功能指标。细胞增殖作为多细胞生物生长、发育、修复和再生至关重要,是维持生命活动的核心过程。细胞以分裂的方式进行增殖,是生物体生长、发育、繁殖和遗传的基础。通过在细胞中过表达或干扰某个基因研究基因对细胞增殖能力的影响,进一步研究基因的功能,或对细胞进行药物处理,研究药物对增殖的影响。
目前常用的细胞增殖检测手段有很多,主要包括: CCK8/EdU检测等方法。
CCK8结果展示图:
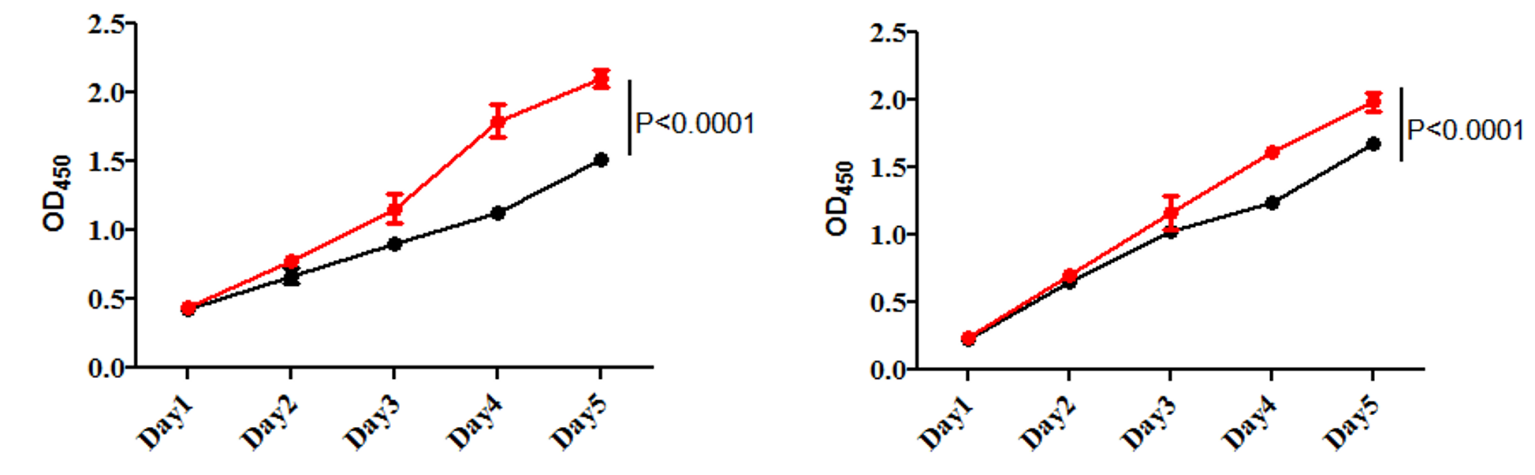
EdU细胞增殖结果展示图:
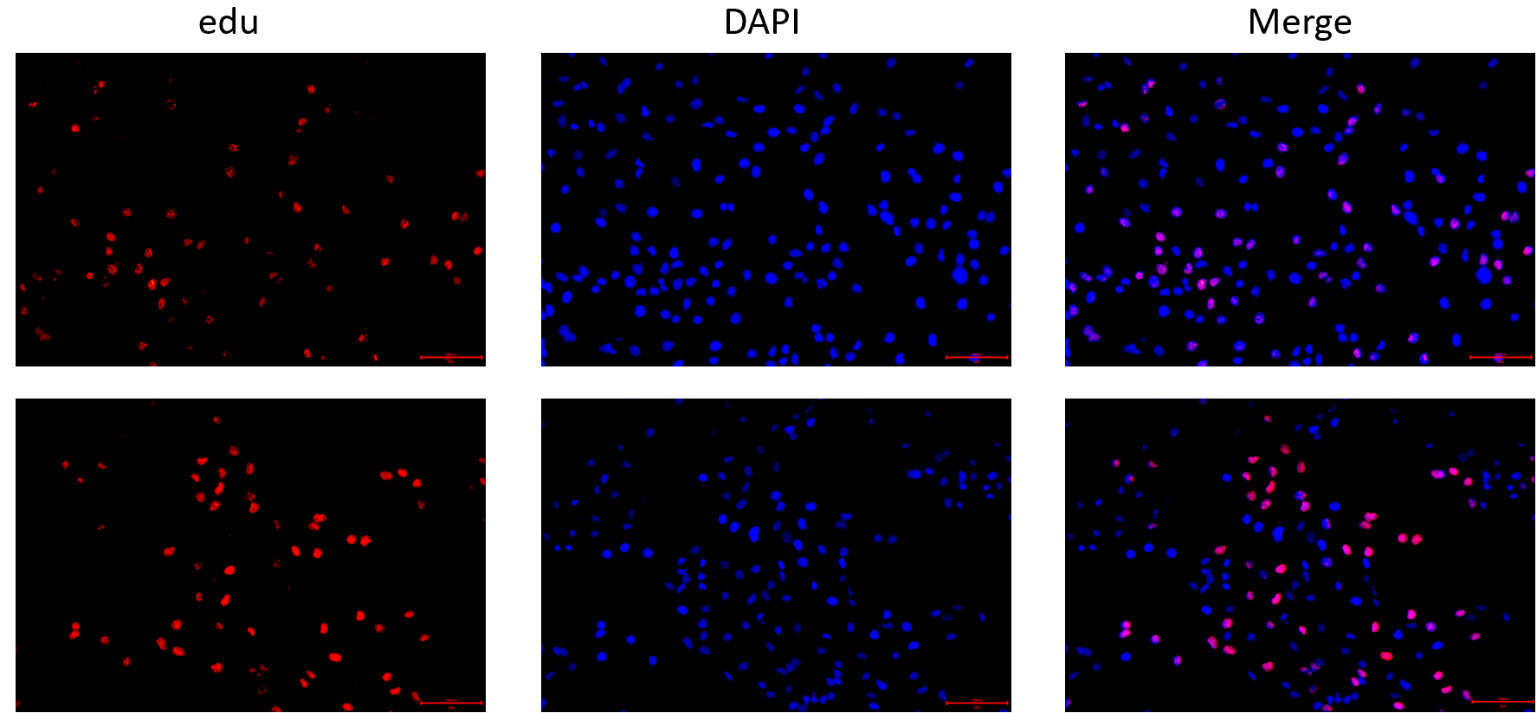
4、细胞凋亡
细胞凋亡(Apoptosis)也称为程序性细胞死亡,是高度调控的过程:不仅除去机体内无需的细胞和组织、使机体正常生长和发育,而且杀死多余的免疫细胞和病毒感染或DNA损伤的细胞、最大地减少对机体的威胁。
细胞凋亡(程序性细胞死亡)在细胞形态和细胞生理上都不同于细胞坏死(损伤性细胞死亡)。与坏死细胞不同,凋亡细胞表现出细胞核染色质紧密、细胞质收缩以及产生膜结合的凋亡小体,而且细胞凋亡还可通过基因断裂以及多种细胞蛋白裂解或降解来与细胞坏死区分。细胞凋亡的失调与多种疾病也相关,包括癌症、中风、阿尔茨海默病和多种自身免疫性疾病。
凋亡结果展示图:
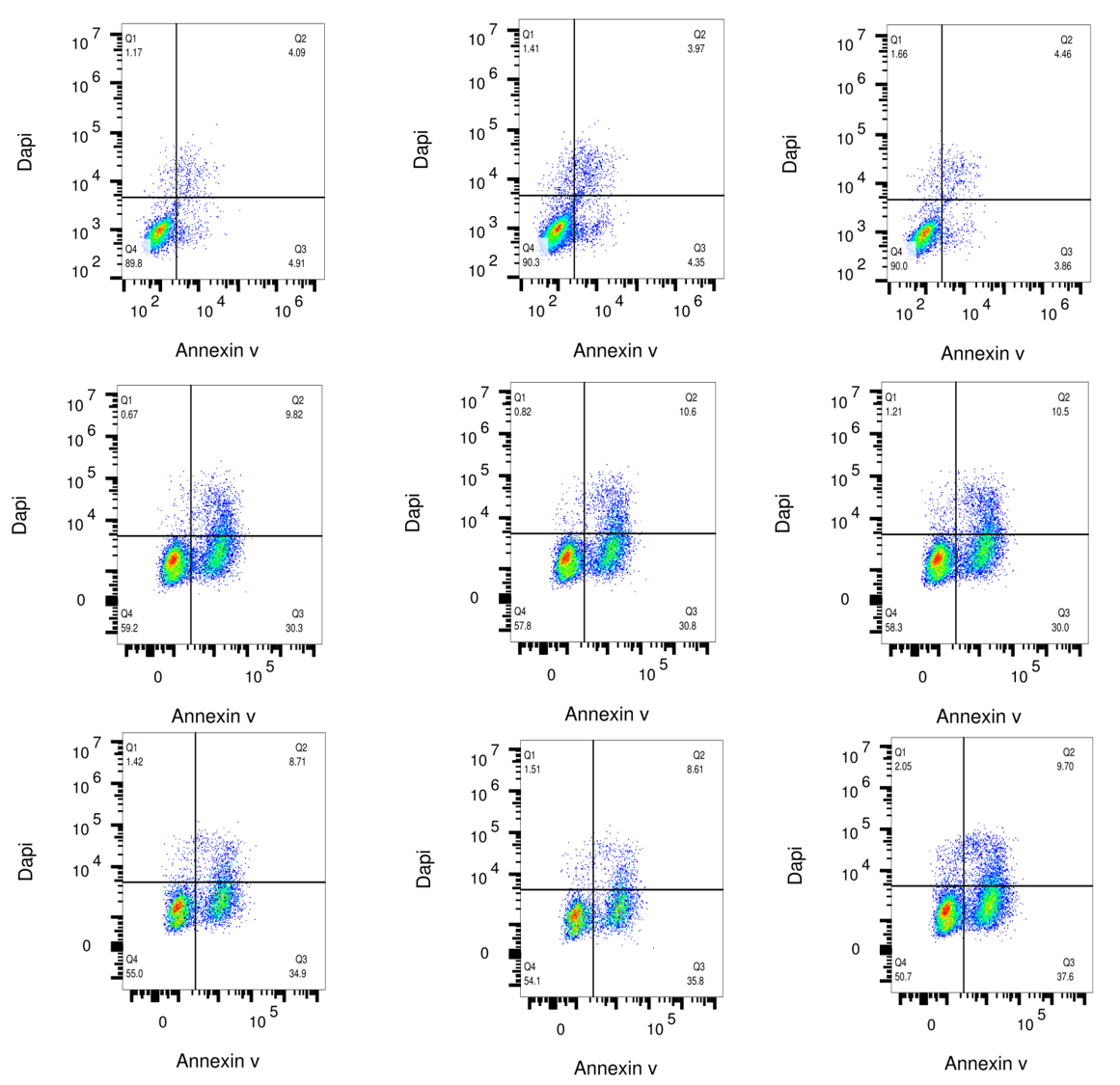
5、Transwell
细胞迁移(Cell migration):也称为细胞移动、细胞爬行或细胞运动,是指细胞在外界信号的作用下从一个位置(区域)移动到另一个位置(区域)的过程,这个过程在生物体内发挥着非常重要的生理和病理学作用,比如损伤修复、肿瘤转移、免疫细胞的迁移、组织修复等。
常用的细胞迁移实验方法是细胞划痕实验。
细胞划痕实验(Cell scratch assay)是通过在细胞单层上划痕并通过延时显微镜定期捕获图像,从而研究细胞迁移运动、修复能力和细胞间相互作用的实验室技术,基本原理是:在融合的单层细胞上人为制造一个空白区域,称为“划痕/伤口”,划痕边缘的细胞会逐渐进入空白区域使“划痕/伤口”愈合,于细胞迁移过程中在开始和定期捕获图像,通过测量不同时间点的划痕间距并计算差值,可对细胞的迁移能力做出判断。因其类似体外伤口愈合过程,又名伤口愈合实验(Woμnd healing assay)。可用于可以观察药物、基因等外源因素对细胞迁移、修复和相互作用的影响。
Transwell结果示例图:
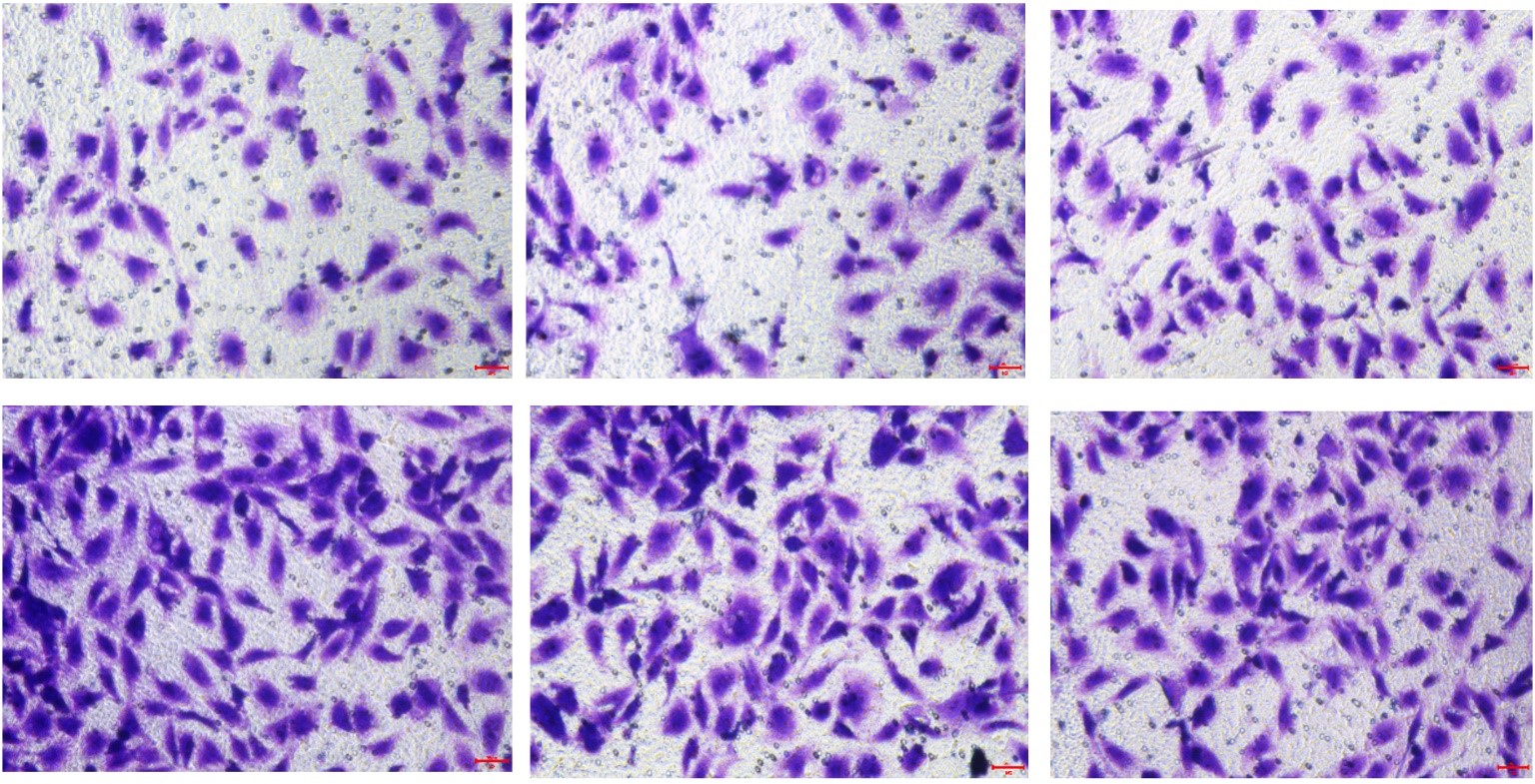
6、稳转株构建
稳转株构建是一种生物学技术,旨在创建能够在细胞中稳定表达外源DNA的细胞株。这通常涉及将目的基因或shRNA克隆到带有特定抗性标记的载体上,然后将这个重组载体转染到宿主细胞中,并整合到宿主细胞的基因组中。随后,通过药物筛选等方法,选择出能够稳定传递外源DNA的细胞株。
一、稳转株构建常用方法
(1)质粒直接转染。使用脂质体等试剂将质粒DNA转染到细胞中,然后通过抗生素筛选等方法筛选出稳定整合了外源DNA的细胞株。
(2)慢病毒侵染。利用慢病毒载体将目的基因或shRNA转染到细胞中,慢病毒载体能将DNA整合到细胞基因组中,从而实现稳定表达。这种方法适用于各种类型的细胞,且整合效率高。
二、稳转株构建流程
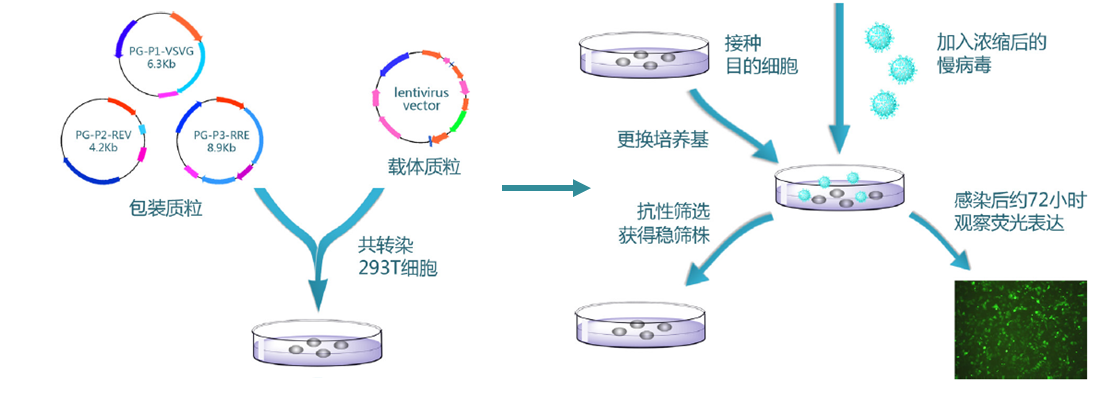
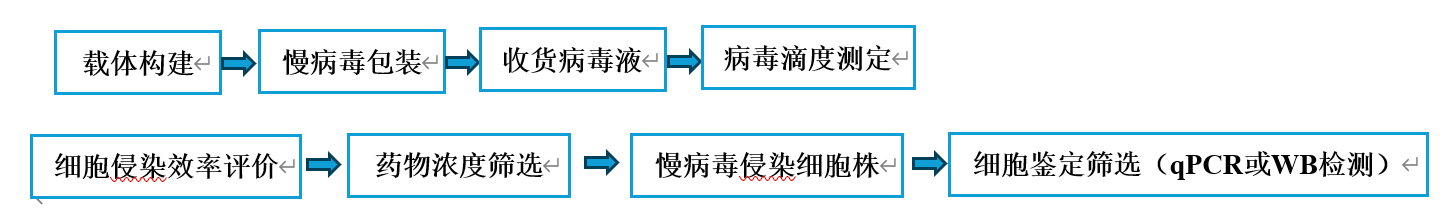
三、稳转株筛选实验方法
(1)侵染效率评价
侵染效率是指成功侵染的细胞数与总细胞数的比例。可以通过显微镜观察侵染后的细胞数量来计算转染率。利用带荧光的NC对细胞进行侵染,正常18-24小时换液,侵染3天后荧光显微镜观察拍照(荧光+明场细胞图片)
(2)最小致死浓度筛选
确定抗生素作用的最佳浓度:不同的细胞株对各种抗生素有不同的敏感性,因此在筛选前要做预试验,确定抗生素对所选择细胞的最低作用浓度。
③ 培养 3-7天以绝大部分细胞死亡浓度为准,一般为 1μg/ml(以嘌呤霉素为例),筛选稳定表达克隆时可比该浓度适当提高一个级别维持时使用筛选浓度的一半。
(3)稳转株筛选正式实验
按照侵染效率评价70%以上阳性的病毒用量进行侵染,侵染48h-72h可以先观察荧光,侵染72h收取瞬时侵染样进行WB或QPCR检测,按照最小致死的浓度开始加药筛选,正常筛选1-2周,荧光全亮且WB或QPCR检测正常即为稳转株。
7、FISH实验
产品简介
基安生物可以定制合成多种荧光标记的FISH探针等。荧光标记的FISH探针可以搭配相关的荧光原位杂交(FISH)试剂盒一起使用,结合激光共聚焦显微镜可用于对目标RNA的细胞定位检测等用途。
|
荧光FISH探针
|
5nmol
|
|
DEPC水
|
250ul
|
表1 20μmol/L的荧光FISH探针储存液的配置参考
|
常见的荧光染料类型
|
激发波长
|
发射波长
|
颜色
|
|
FAM标记
|
495 nm
|
520 nm
|
Green/yellow
|
|
Cy3标记
|
550 nm
|
570 nm
|
Darkpink/Red
|
|
Cy5标记
|
650 nm
|
670 nm
|
Far red
|
表2 常见的几种荧光FISH探针
基安生物可提供miRNA,mRNA,lncRNA,circRNA,FISH探针设计,细胞样本FISH实验,动物组织石蜡切片FISH实验,动物组织冰冻切片FISH实验。
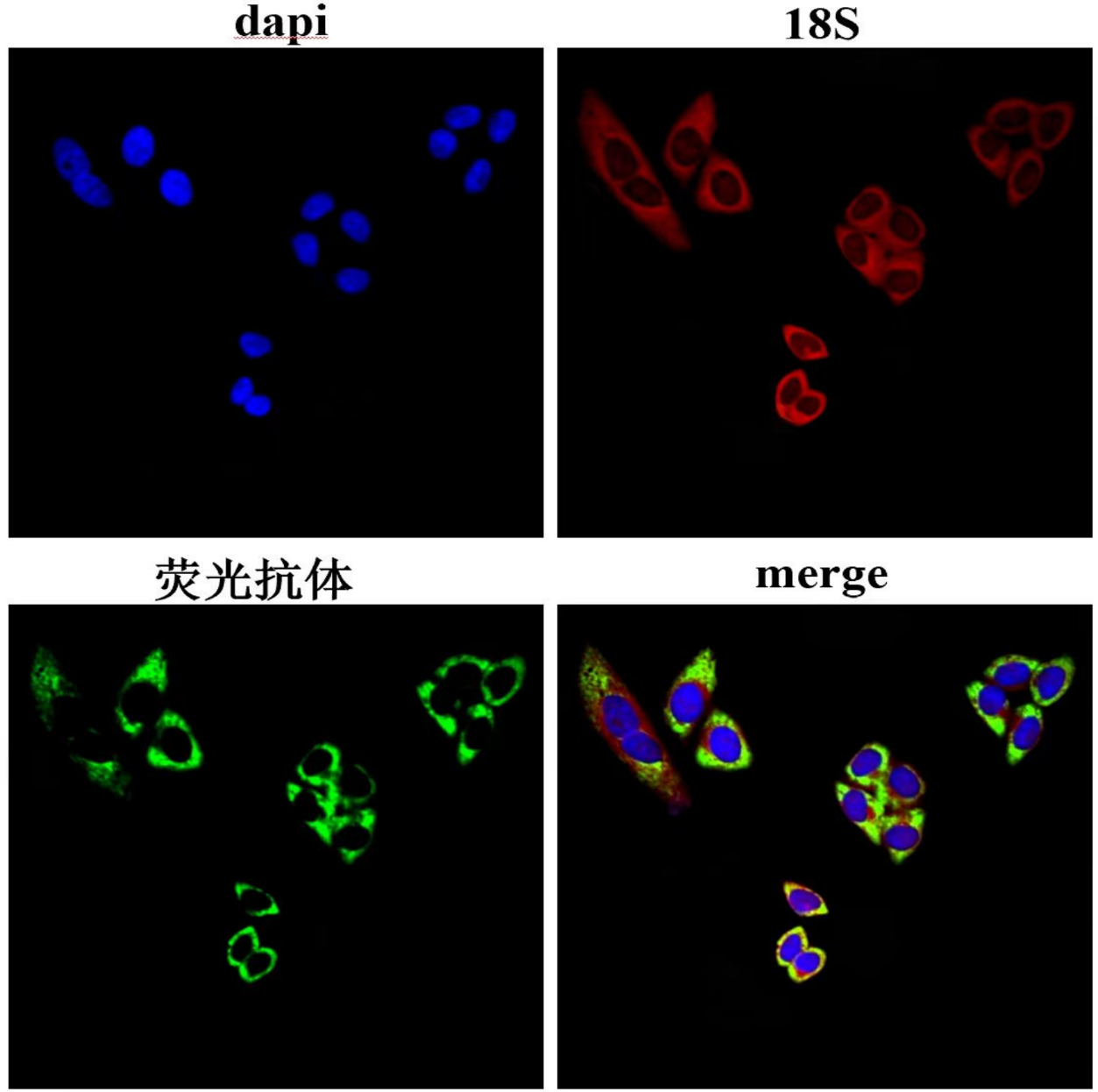
FISH结果示例图:

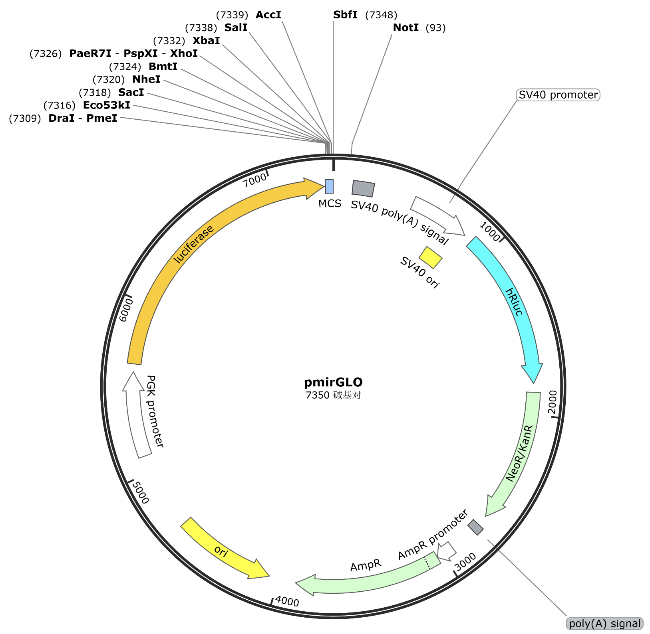
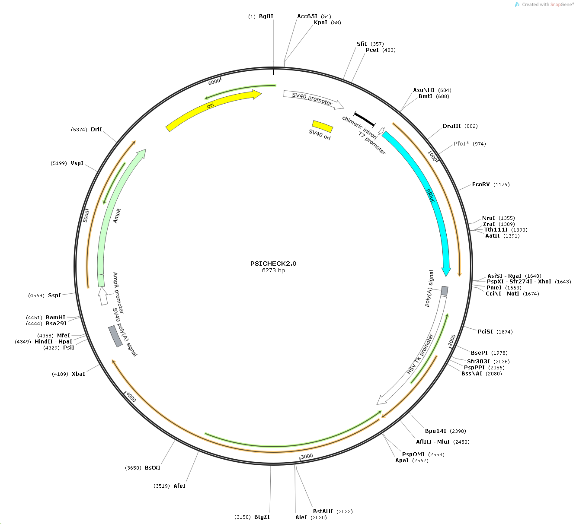 psiCHECK2.0载体
psiCHECK2.0载体