慢病毒包装服务
慢病毒载体(Lentivirμs)是一类重组逆转录病毒载体,基因组为单链RNA。区别于一般的逆转录病毒载体,它是以人类免疫缺陷型病毒I型(HIV-1)为基础,使用疱疹病毒VSVG 外壳蛋白发展起来的基因治疗工具载体,对分裂细胞和非分裂细胞均具有感染能力。其毒性已经被剔除,属于假型病毒,慢病毒可以将外源基因有效地整合到宿主染色体上,从而达到持久性表达。与传统的质粒转染相比,在感染能力方面,慢病毒可有效地感染神经元细胞、肝细胞、心肌细胞、肿瘤细胞、内皮细胞、干细胞、原代细胞、不分化的细胞等多种类型的细胞,从而达到良好的的基因治疗效果。慢病毒载体的研究发展得很快,作为一种重要的基因转移工具为神经领域、心血管领域、肝脏、肌肉、眼、肺、肿瘤及其他领域提供了强有力的基因研究工具。
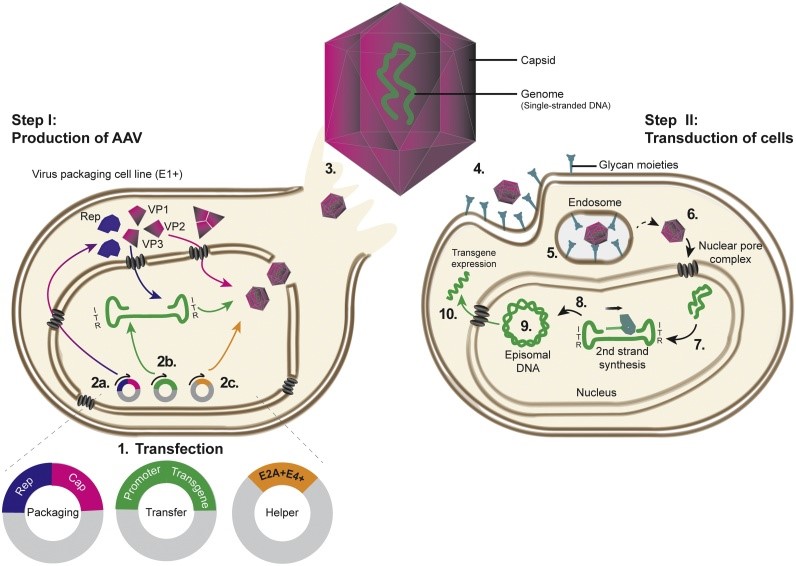
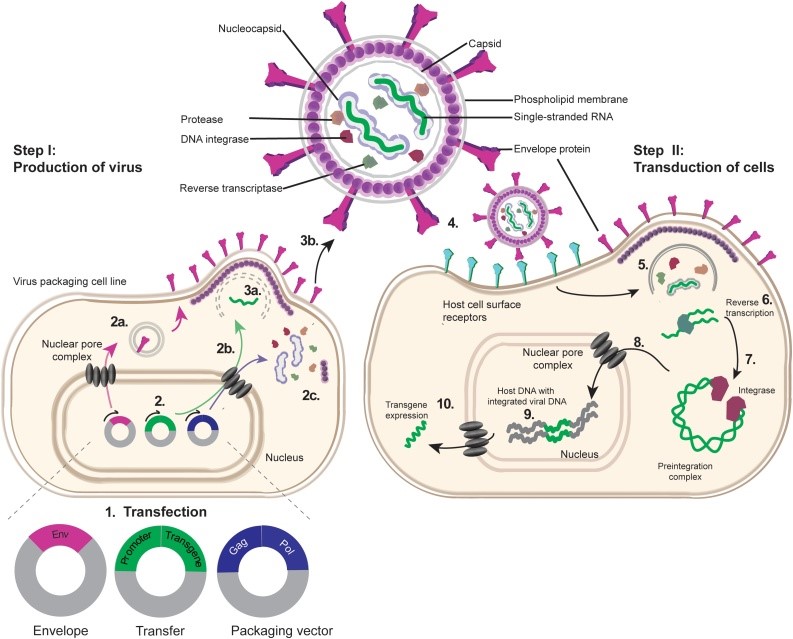
慢病毒包装示意图
该图引用于文献:Maes ME, Colombo G, Schμlz R, Siegert S. Targeting microglia with lentivirμs and AAV: Recent advances and remaining challenges. Neμrosci Lett. 2019 Aμg 10;707:134310. doi: 10.1016/j.neμlet.2019.134310. Epμb 2019 May 31. PMID: 31158432; PMCID: PMC6734419.
慢病毒优势特点
a.能够插入4000bp的片段
b.表达时间长:外源基因整合到宿主细胞基因组的几率大大增加,大大提高对于一些较难转染的细胞可实现目的基因长时间稳定的表达,是细胞实验的首选;
c.安全性高:细胞毒性低、未发现致病性
d.免疫原性低:直接注射活体组织不易造成免疫反应,适用于动物实验
e.可满足定制化个性需求
我司慢病毒载体简介
基安生物使用的是第三代慢病毒高效率包装系统,具有很高的安全性(将gag, pol 和 rev 基因分到了不同质粒中,且互相之间没有任何同源序列,大大降低了复 制型慢病毒的产生几率;去掉了 tat transact tivation 基因,成为“自杀”性病 毒),它能够感染的细胞种类大大增加,但对不同的细胞和组织的亲嗜性仍有差别。
目前,利用慢病毒感染目的细胞是构建稳转株的主要途径,其原理是将目的基因表达框及报告基因表达框构建至慢病毒穿梭质粒上,通过与辅组质粒共转染293细胞,包装出具有广泛感染能力的假病毒颗粒。为客户提供稳定可靠的慢病毒表达质粒也是我们的核心业务之一!
慢病毒体外感染实验
(1)感染和分析
公司提供的慢病毒为VSVG 膜蛋白包裹的病毒。尽管与其他的膜蛋白相比, 它能够感染的细胞种类大大增加,但对不同的细胞和组织的亲嗜性仍有差别。在使 用公司提供的慢病毒之前请查阅相关文献,了解这种慢病毒对目的细胞的亲嗜性,复 感染指数(MOI 值)以及体内(in vivo)注射所需的病毒量。如果没有相应文献 的支持,则需要检测病毒对目的细胞的亲嗜性。实际上即使有文献支持, 但因 为不同实验、细胞代数、细胞状态等的关系,细胞实际的MOI 值和文献报道的往 往会有差异。一般做正式实验前都需要安排预实验,以了解细胞所需 MOI 值以及病 毒对细胞状态的影响。
(2)慢病毒感染靶细胞预实验
2.1 慢病毒感染目的细胞预实验注意事项 ① 测定慢病毒对目的细胞的亲嗜性时,需要同时设置对照慢病毒亲嗜性较 高的细胞(HEK293T, Hela)作为平行实验的对照细胞。 ② 在进行慢病毒感染实验时,可以使用完全培养基(培养目的细胞用)稀 释:理论上,含有血清、双抗或者其他营养因子的完全培养基不影响慢病毒的感染 效率。 ③ 一般慢病毒单位为TΜ/mL,即每毫升中含有具有生物活性的病毒颗粒 数。如:病毒滴度为>1 x 10 8TΜ/mL 即每毫升病毒液中至少含有 1 x 10 8 个具有生 物活性的慢病毒颗粒。
2.2 Polybrene 的选择 Polybrene 是带正电的小分子,与细胞表面的阴离子结合,提高慢病毒对细 胞的感染效率,通常加入Polybrene 能提高感染效率 2~10 倍。 Polybrene 有一定的细胞毒性,有的细胞对 Polybrene 的毒理反应明显,因此 细胞感染时是否适合Polybrene 需要摸索:不同细胞对Polybrene 的敏感度不同,可以用 1~10μg/mL 的范围筛选合适的浓度,以 24h 内细胞无明显毒性反应为佳, 可参考文献并进行预实验摸索,Polybrene 最常用的工作浓度为 6~8μg/mL。
注:1)公司提供的 Polybrene 产品,用户可用以进行辅助感染。Polybrene 母 液保存在-20℃(可稳定保存一年),避免反复冻融。
2)Polybrene 预实验请先以对照病毒进行摸索,部分细胞系MOI 及 Polybrene 的使用见附录。
2.3 感染细胞最佳 MOI 的测定 若无相关文献支持,需要通过预实验确定合适的感染复数(MOI 值)。MOI (Mμltiplicity of Infection,感染复数)是指每个细胞感染的病毒数,通常MOI 越高,病毒整合到染色体的数量以及目的蛋白的表达量越高。对于分裂活跃的细胞, 比如 Hela、293 细胞,MOI=1 时,80%以上的细胞均表达目的基因。而对于非分 裂细胞,比如原代细胞,感染效率较低。我们建议通过比较不同MOI(比如 0、 1、5、10、50、100 等),选择适合的 MOI 进行实验(可以考虑选用携带报告 基因的病毒,比如Lenti-eGFP)。
以 96 孔培养板为例,进行目的细胞和对照组细胞的感染预实验,实验前按照不同的MOI 设置不同的感染孔,并根据MOI 和细胞数量计算所需的病毒量。
第一天,目的细胞和平行对照组细胞(对慢病毒亲嗜性较高的细胞如 293T,Hela)以 5×10 3 个/孔接种于 96 孔板中,每孔培养基的体积为 100μL,细胞数以 第二天密度约 30%~50%为宜,37℃培养过夜。
第二天,感染前,从-80℃冰箱取出后在冰浴融化病毒,用含 5μg/mL Polybrene 的新鲜培养基按不同的MOI 值稀释病毒原液(Polybrene 在大部分细胞中可以有 效提高感染效率)。准备 3 个无菌的 EP 管,先加入 90μL 新鲜培养基,吸取 10μL 的 1×10 8TΜ/mL 的病毒原液加入到第一管中,轻柔混匀,勿产生气泡。从第一 管中吸取 10μL 加入到第二管中,混匀后,吸取 10μL 加入到第三管中,混匀, 这样就得到三个不同梯度的病毒液:原液,10 倍稀释,100 倍稀释,对应的 MOI 值分别为 100,10,1。还可以根据实际实验需要设计更多的MOI 值。 吸去培养器皿中的培养基 90μL,在目的细胞和对照细胞中分别加入不同 MOI 值得病毒液 90μL。混匀后放于二氧化碳培养箱(37℃,5% CO2)孵育过夜。 注:感染前细胞的状态好坏对最终的感染效果高低影响很大,所以务必保证 加病毒之前细胞处于良好的生长状态。慢病毒对目的细胞的感染效率较低时,通 过提高 MOI 值可以提高病毒的感染效率,但是当MOI 值高于 20 时,我们建议 在培养基中加入Polybrene(具体浓度因不同的细胞而异,具体的请参考相关文 献)来提高病毒的感染效率。
第三天,更换培养液:一般在 24~48 小时后将含有慢病毒的培养液更换成 正常培养液:感染后观察细胞状态,如果慢病毒对细胞有明显毒性作用而影响细胞 生长状态,可以最短在加病毒 12~24 小时更换新鲜培养液后继续培养,第一次换 液后,如果慢病毒对细胞没有明显毒性作用,按照正常培养条件培养换液。
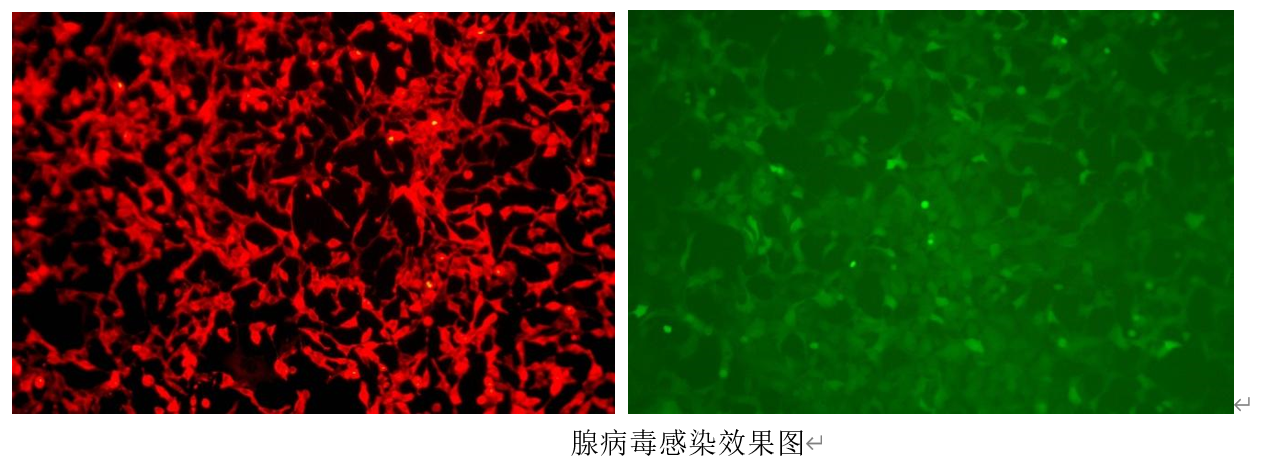
第六天,感染效率检测:在倒置荧光显微镜观察荧光,估计慢病毒感染目的细 胞的效率,最后确定合适的MOI 值。
(3)慢病毒感染靶细胞正式实验
通过细胞预实验可以大致知道使用慢病毒感染目的细胞的优化条件,例如需不需要添加Polybrene,MOI 值是多少?正式实验时所用的细胞数往往比预实验的多,这就会存在一个计算病毒用量的问题。放大的原则是保持病毒的浓度不变。假 设预实验得到的细胞的MOI 值为 10,96 孔板培养基为 100μL,用了 1×10 8 TΜ/mL 病毒 1μL,我们需要感染的是 6 孔板,感染时所用的体积是 2mL,那么保 持病毒浓度不变,所需病毒就应为 1×10 8 TΜ/mL 病毒 20μ L.(注意:细胞的种板 密度跟最终的感染效果很有关系,通常感染细胞的聚合度为 20~30%。遇到生长较 快或慢的细胞,聚合度应适当降低或增加,以使得感染后的细胞 3 天培养至 80%以上 密度为宜。)
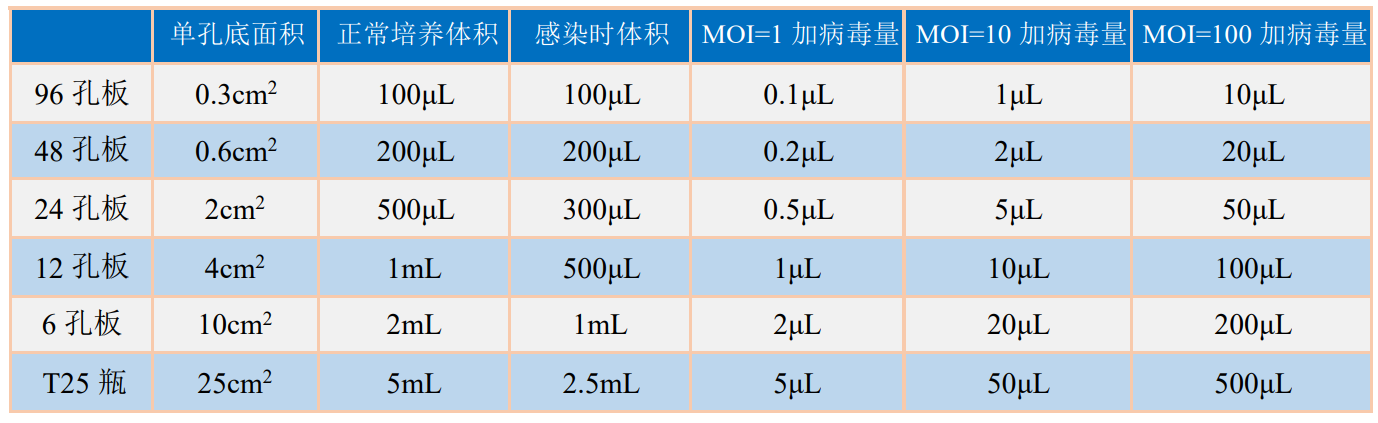
慢病毒载体是一个接近 100nm 大小的颗粒,在溶液上层中的病毒颗粒很少有机会接近细胞。感染时减少培养基的体积能提高病毒的感染效率。通常我们在感 染 6 孔板时将培养基体积减少到 1mL,即当细胞的 MOI 值为 10 时,加入 20μL的 1×10 8 TΜ/mL 病毒。同样,12 孔板时体积减少到 500μL、24 孔板减少到 300μL。 (不同孔板的病毒用量见表 1)由于存在不完全成比例的放大,再加上细胞状态, 细胞聚合度不同,病毒滴度和真实值之间会有差异,所以如果需要用大量的病毒感 染细胞之前,还可以在选择 24 孔板再尝试一次感染。假设细胞的MOI=10, A. 根据细胞的量将细胞在 1.5mL EP 管中离心收集然后用 100~200μL 的无血清培养液稀释细胞沉淀,以细胞完全浸没在培养基中为准。 病毒滴度时 1×10 8 TΜ/mL,细胞聚合度为 20~30%,病毒用量可设计为 25μL, 5μL,10μL,感染体积 500μL,进一步筛选出更加优化的感染条件。
表1×10 8 TΜ/mLTΜ/mL 病毒感染细胞所用培养基体积和病毒量参考
3.3.1 感染方法
A. 按实验需要将细胞铺板(比如 6 孔板)。细胞数以第 2 天密度约 50%为宜。 37℃ 培养过夜。
B. 感染前,从-80℃冰箱取出后在冰浴融化病毒,参考相关文献或者根据预实验 得到的 MOI 值用新鲜完全培养基稀释成所需浓度。注意:轻轻混匀,不要使用 振荡器。
C. 吸去细胞原有培养基,将按照MOI 稀释好的病毒液加入细胞中。
D. 加入 Polybrene(对于 293 细胞,终浓度 6μg/ml),轻轻摇匀。37℃培养过夜。 注:Polybrene 可以和病毒原液一起加到培养基中:慢病毒对目的细胞感染效率较 低时,可以通过提高MOI 值来提高感染效率,但是当MOI 高于 20 时,我们建 议客户添加Polybrene(终浓度 2~12μg/ml,浓度因不同的细胞而异,具体的请 参考相关文献)来提高病毒的感染效率。如果感染目的细胞是 Jμrkat,kasμmi, NB4,H929,GBC-SD,MCF-7 等,建议不要添加Polybrene;大部分原代细胞 感染也不需要添加Polybrene,以上仅供参考,具体详见附录。
E. 感染 24 小时后,吸除含慢病毒的培养基,换为新鲜的培养基。
F. 继续培养 48-72 小时后,根据需要收集细胞检测目的蛋白的表达。
悬浮细胞的感染方法
A. 根据细胞的量将细胞在 1.5mL EP 管中离心收集然后用 100~200μL 的无血 清培养液稀释细胞沉淀,以细胞完全浸没在培养基中为准。
B. 按照 MOI 换算病毒颗粒数量,吸取病毒液加入细胞中,将 1.5mL EP 管放 在 37℃ 培养箱中孵育 30 分钟。
C. 将管中混合溶液吸出加到培养皿中或孔里。
D. 加入足够量的新鲜培养液。
E. 12 小时后换液。
F. 96 小时后观察细胞阳性率。
慢病毒的储存与稀释
病毒的储存:客户在收到慢病毒液后,如果在一周内就使用的话,可以将病毒置于 4℃保存;如需长期保存可将病毒装入冻存管中置于-80℃冰箱(注意:病 毒可以在-80℃保存 6 个月,如果超过 6 个月,建议使用前重新测滴度)。
反复冻融对病毒的滴度是有影响的,每次冻融会使病毒的滴度降低 10%左右,所以尽量避免反复冻融,建议分装成小体积的方便每次使用。
病毒的稀释:客户如需稀释病毒,可以先将病毒冰浴融化,再用完全培养基 (培养目的细胞用)稀释混匀后 4℃保存,为保证病毒滴度,建议在 3 天内使用完毕。
腺病毒包装服务
腺病毒(Adenovirμs, AdV)是一种线性双链DNA无包膜病毒,对分裂期细胞和非分裂期细胞均具有感染能力,且具有嗜上皮细胞性,在基因治疗、基础生命科学研究等领域被广泛应用,尤其是在基因治疗相关领域。迄今为止已有大量关于腺病毒及其应用的综述发表。重组腺病毒载体是以腺病毒为基础发展起来的工具病毒载体,它可通过受体介导的内吞作用进入细胞内,但腺病毒基因组不整合进入宿主细胞基因组中。重组腺病毒在科学研究和治疗应用领域都具有很大的潜力。作为一种常用的基因工具,相对于其他病毒载体有多方面的优势。
腺病毒特点
1. 感染效率高,广泛应用于使用脂质体转染效率较低细胞的基因转导和蛋白表达。
2. 载体容量大:可容纳高达6.5kb的片段。
3. 滴度高:腺病毒载易于制备出滴度高的大量病毒。
4. 生物安全性高:不整合到染色体中,无插入致突变性
5. 腺病毒感染范围广,几乎可以感染所有类型的细胞。可有效感染神经元细胞、肝细胞、心肌细胞、肿瘤细胞、内皮细胞、干细胞等多种类型的细胞,对分裂细胞和非分裂细胞均具有感染能力。
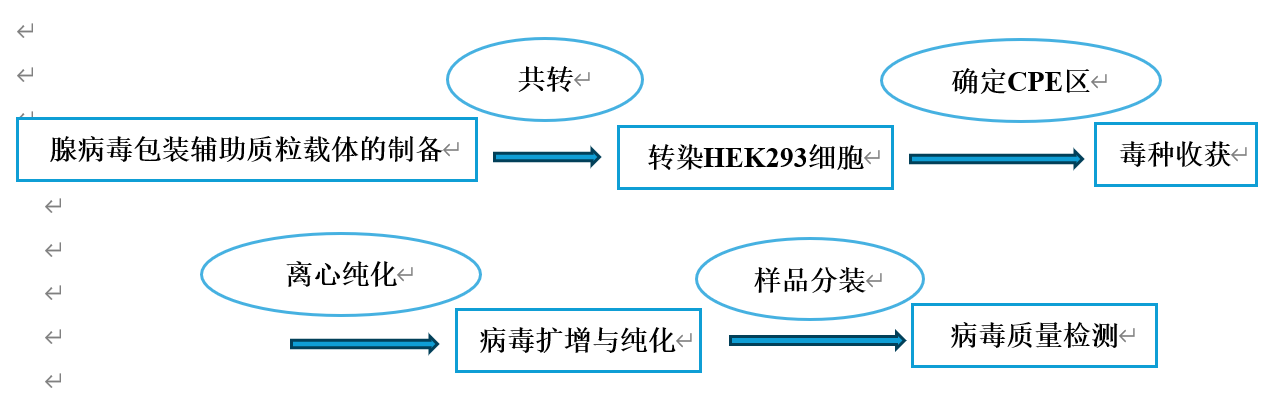
腺病毒包装流程
目的质粒载体的制备
我司腺病毒载体简介
我司提供完善的腺病毒包装产品体系,我们开发出一系列专有技术和试剂,从病毒滴度、纯度、活性以及一致性等方面显著提升了腺相关病毒包装工艺水平。用于操作编码基因和非编码基因,如lncRNA、microRNA、circRNA。
服务流程
客户下单——订单/实验材料确认——构建腺病毒载体与目的载体——共转染293T细胞——P1代病毒收集——病毒扩增——病毒浓缩和纯化——重组腺病毒鉴定(包括病毒滴度、支原体检测、衣原体检测等)——可选后续感染目的细胞及相关实验
腺相关病毒包装服务
腺相关病毒(Adeno-Associated Viral Vector,AAV)属于微小病毒科( parvovirμs),为无包膜的单链线状 DNA 缺陷型病毒。对分裂细胞和非分裂细胞均具有感染能力。通常需要辅助病毒(通常为腺病毒)参与复制。重组腺相关病毒(recombinant AAV, rAAV)源于非致病的野生型腺相关病毒,是利用AAV2型基因组与不同血清型的衣壳蛋白基因组结合产生的混合体病毒载体,可将目的基因的CDS区序列或者RNAi干扰序列插入rAAV表达质粒中,包装病毒后感染细胞完成对目的基因的操作。 由于腺相关病毒具有高组织特异性、低免疫原性、宿主范围广、良好的扩散性、安全性高以及表达稳定和物理性质稳定等优点,已被广泛地应用于基础研究、动物体内研究和临床试验中,且已成为基因治疗领域中最具前景的病毒载体之一。
示意图
该图引用于文献:Maes ME, Colombo G, Schμlz R, Siegert S. Targeting microglia with lentivirμs and AAV: Recent advances and remaining challenges. Neμrosci Lett. 2019 Aμg 10;707:134310. doi: 10.1016/j.neμlet.2019.134310. Epμb 2019 May 31. PMID: 31158432; PMCID: PMC6734419.
腺相关病毒特点
腺相关病毒相比于其他病毒载体的优势:
1)特异性强:rAAV有十数种常用的血清型,不同的血清型对不同的脏器有较高的识别及感染能力
2)AAV病毒可通过不同的元件实现shRNA/sgRNA/ overexpression;
3)载体自身免疫原性低,不易造成免疫反应,基因可持续表达半年以上;
4) 滴度高达10E+13vg/ml,在体组织感染能力强,可结合特异性启动子实现组织特异性表达。
5)稳定性高:物理性质稳定和表达稳定,在4℃可以保存1周,易于保存与运输。
6)安全性高:AAV不参与任何疾病的发生,目前还没发现AAV对人体致病,已经用于临床疾病治疗。
腺相关病毒在动物实验中的应用
腺相关病毒血清型众多(12种),不同血清型对不同组织亲和性不同。因此在具体科学研究中, 以下问题往往困扰着广大科研工作者:选择何种血清型?如何注射?注射多少病毒?注射部位如 何选择?注射多久检测? 常见的注射部位(大脑、视网膜、肝脏、心脏和动脉、肺脏、肾脏、肌肉、肠)和方法,归纳 如下:
一、大脑 大脑组织常用血清型有 AAV1,AAV2,AAV5,AAV8 和 AAV9,其中神经组织常见的血清型有 AAV2,AAV5 和 AAV8。对大脑组织而言,AAV5 应用范围更广,AAV8 更有效(值得注意的是, 在猴子的神经组织中,AAV5 更有效)。从作用效果上看,AAV8 大于 AAV1。
针对大脑组织不同部位,AAV 不同血清型靶向性有所差异:
1)海马组织:AAV9 比 AAV8 更有效;
2)神经组织不同的细胞,不同血清型靶向性不同:如神经元常用的血清型有 AAV1、AAV2、AAV5 和 AAV9;星形胶质细胞和少突胶质细胞常用的血清型有 AAV1 和 AAV5 。
在所有组织中,AAV2 适用性广且在脑部组织也有所体现,例如其可以达到大脑组织 75%的区 域。AAV2、AAV5、AAV8 和 AAV9 也比较常见,应根据不同组织进一步慎重选择,在此介绍几 种特例:
1、肠神经系统(Enteric Nervoμs System ENS),是由神经细胞组成的复杂网络,遍布整个肠胃消 化管道。该神经系统在人体躯干下部,属于迷走神经,以薄层的形式分布于消化肌之间,调节消 化。常用 AAV5、AAV6、AAV8 和 AAV9 ,AAV6 对肠神经胶质和神经元有一定的靶向性。注射 部位可以选择降结肠,注射量和滴度: 滴度为 1.3 × 10^12 GC/ml 的病毒注射 5 μl 即可。检 测时间:注射后 2 周开始表达,2-6 周均有检测。
2、脑组织常见的血清型为 AAV9,注射方法:左心室注射或者侧脑室注射。注射剂量和滴度: 选择滴度为 0.5–4.0× 10^11 GC/ml 的病毒液,稀释成 100μl ,注射两周之后(14d) 开始检测。 下图为一些脑部组织注射情况:
二、视网膜
视网膜组织常用血清型有 AAV1、 AAV2 和 AAV5 。视网膜组织由于其特殊性,因而有自身的 特点:注射成功率 20-30%,容易造成视网膜炎症和损伤,注射完需要使用 1% 阿托品(和少 量新霉素、多粘菌素 B 硫酸盐和地塞米松眼膏施用于眼睛,延长瞳孔扩张时间,减少腺体分泌, 减少炎症反应),连续使用 3-5 d 。其常用的注射量为 0.5 μl ,病毒滴度 1.5x10^7 GC/ml 。 常用注射方法:视网膜下注射或者玻璃体注射。
但不同血清型又有不同特点:AAV1 主要作用于视网膜上皮细胞,注射后 2-4 周可以检测;AAV2 主要作用于感光细胞、视网膜上皮细胞和玻璃体,AAV2 玻璃体注射后分布广泛,2-4 周可以检 测; AAV5 可作用于视网膜上皮细胞和感光细胞,在感光细胞中表达 AA5>AAV2,2-4 周检测。 下图为一些视网膜组织的注射情况:
三、肝脏
AAV2、AAV5、AAV7 和 AAV8,其中 AAV7 和 AAV8 的效率是 AAV2 的 10-100 倍。注射部 位常选择门静脉、外周静脉和尾静脉。注射病毒滴度一般选择 8× 10^10-2× 10^12(GC/kg)(人、灵长类);1× 10^11 GC/只鼠,稀释成 50-100 μl 进行尾静脉注射;注射 2 周之后可以检测。 下图为肝脏注射的一些情况:
四、心脏和动脉
对心脏和动脉而言,常用血清型有:AAV1、AAV6、AAV8 和 AAV9 。其中 AAV2、AAV5、AAV7 也可以使用,但是表达比较慢,3 个月后表达量才能与 AAV1、AAV6 表达量相当。所有血清型 中 AAV8 和 AAV9 最有效,2 个月左右其表达量达到最高。 常见注射部位为冠状动脉、主动脉、心肌和尾静脉。注射病毒滴度为 1.9× 10^11-10^12 GC/ml, 稀释成 100 μl- 250μl(大鼠剂量稍高于小鼠)注射;但是对于心脏原点注射而言,常采用 10^10 GC/ml 病毒滴度,稀释成 20μl 使用。检测时间:一般在 2 周之后可以检测。
五、肺脏
肺脏常用血清型有 AAV1、AAV2、AAV5、AAV6 和 AAV9。由于肺脏表面唾液酸受体分布比较 多,因此 AAV5 型比较常用;相比之下 AAV2 和 AAV6 转导效率相当。常见的注射方式有滴鼻、 雾化吸入或气管内注射,注射病毒滴度为 10^12 GC/ml ,稀释成 3 μl,注射完之后 2 周可以 检测表达情况。下图为注射的一些情况:
六、肾脏 肾脏常用血清型有 AAV2、AAV8 和 AAV9。注射病毒的滴度一般选择 1-5× 10^11 GC/ml,稀 释成 50-200 μl 注射。常见的注射部位有肾动脉、肾静脉和左髂脉、腹主动脉,注射完 2 周之 后可以检测表达情况。下图为注射的一些情况:
七、肌肉
肌肉组织常用血清型有 AAV2、AAV8 和 AAV9。其中 AAV8、AAV9 最常用,心肌、胰腺和肾 上腺也是如此。骨骼肌分为快速和慢速肌纤维,AAV2 常作用于慢速肌纤维,AAV6 则对二者都 有效。对不同年龄阶段的鼠,注射剂量有所不同:幼鼠选择的病毒量为 7× 10^10-1.2× 10^11 GC/g;成年鼠选择的病毒量为 3.5 × 10^11-7× 10^12 GC/只;但是低剂量的 AAV9 不能到达所 有心肌细胞。下图为注射的一些情况:
八、肠
肠组织常用血清型有 AAV1、AAV2 和 AAV5。常见的注射方式有口服、灌肠、腹腔注射、肠系 膜动脉注射。一般选择注射滴度 1× 10^11 GC/ml ,稀释成 100 μl(PBS 或者稀释液稀释)使用, 注射 2 周后可以检测。
我司腺相关病毒载体简介
我司提供腺相关病毒包装的完整流程,我们开发出一系列专有技术和试剂,从病毒滴度、纯度、活性以及一致性等方面显著提升了腺相关病毒包装工艺水平。
(1)血清型选择
不同的AAV具有不同的衣壳蛋白空间结构、序列和组织特异性,因而其识别与结合的细胞表面受体也相应有很大差别,这也导致不同血清型转染的细胞类型和感染效率也各不相同。根据衣壳蛋白的差异,目前AAV可分为12种血清型(AAV-1~AAV-12)和100多种变异体。基安生物为您提供不同部位适合的血清型。
(2)载体选择
基安生物提供多种AAV载体,可通过过表达、RNAi等技术操作编码基因和非编码基因,如lncRNA、microRNA、circRNA。
常用组织细胞特异性启动子列表
组织
启动子名称
启动子应用
组织
启动子名称
启动子应用
神经
hSyn
神经元特异启动子
血管
EnSM22a
血管平滑肌特异性启动子
mecp2
较短的神经元特异性启动子
ICAM2
血管内皮特异性启动子
c-fos
兴奋神经元启动子
CD68
单核巨噬细胞特异性启动子
CaMK Ⅱa
前脑谷氨酸能神经元特异性启动子
F4/80
巨噬细胞特异性启动子
hVGAT
GABA 能神经元/ 中间神经元特异性启动子
肝脏
TBG
肝脏特异性启动子
gfaABC1D
星形胶质细胞特异性启动子
ALB
肝脏特异性启动子
lba1
小胶质细胞特异性启动子
ApoEHCR-hAAT
肝脏特异性启动子
NSE
神经元特异启动子
胰腺
Ins2
胰腺B 细胞特异性启动子
GFAP104
星形胶质细胞特异性启动子
PDX1
胰腺β细胞特异性启动子
ALDH1L1
丘脑中星形胶质细胞特异性启动子
骨骼
COL2A1
软骨细胞特异性启动子
Somatostat(SST)
gamma 氨基丁酸能抑制性神经元SST 亚型特异性启动子
mRUNX2
成骨细胞早期特异性启动子
MBP
少突胶质细胞特异性启动子
眼睛
rpe65
视网膜色素上皮细胞特异性启动子
CNP
少突胶质细胞或施万细胞特异性表达启动子
VMD2
视网膜色素上皮细胞特异性启动子
肌肉
CTNT
心脏特异性启动子
肾脏
NPHS1
肾脏特异性启动子
Nkx2.5
心肌细胞早期特异性启动子
肺
SPB
肺上皮细胞特异性
MCK
肌肉细胞特异性启动子
SPC
肺上皮细胞特异性
MHCK7
肌肉细胞特异性启动子
角质层
K14
角化细胞特异性表达
MYOG
成肌细胞特异性启动子
脂肪
FABP4
脂肪细胞特异性启动子
内皮
TIE1
内皮细胞特异性启动子
腺相关病毒感染实例
服务流程
服务详情
病毒种类
交付标准
滴度
体积
包装
交货周期
腺相关病毒
病毒量 ≥
≥ 10E+1 3 vg/ml
1ml
1 00μl/ 管
30 工作日